Нитрование бензола. Пиротехническая химия: Химия и технология бризантных взрывчатых веществ - Орлова Е.Ю Получение через диазосоединение
Больше трех нитрогрупп в молекулы бензола и толуола нитрованием ввести не удается.
Амино-2-нитротолуол л-Нитро-п-то- луидин сн Л ч/ 1 мн 0, и Толуол Нитрование - восстановление сернистым натром
М. С. Быховская описывает метод раздельного определения бензола и толуола. Нитрованием бензол переводят в динитробензол, а толуол- в тринитротолуол 77
При фракционировании жидкой части катализата было выделено 14,5 г углеводорода с т. кип. -ИГ (756 mai) n 1,4967 df 0,8665. Сопоставление констант этой фракции с литературными данными для толуола показывает, что она состоит из толуола.
Нитрованием этой фракции получен нитропродукт с т. пл. 69° С. Смешанная проба плавления с 2,4-динитротолуолом депрессии не дала.
Производство ксилила. Как мы видели из работ Мартинсена, при введении 2-й метильной группы в ядро быстроту реакции нитрации значительно увеличивается. Быстроту реакции нитрации ти-кси-лола в раз больше, чем толуола.
Поэтому и смеси для нитрования ксилола могут быть значительно слабее, чем для нитрования толуола. Этим же обусловлено то, что ксилол можно даже в заводских условиях нитровать в тринитроксилол в одну фазу , в то время как для толуола нитрование в одну фазу никогда и нигде не производилось, вследствие того, что это сопряжено с огромным расходом кислот, а потому неэкономично, не говоря о других трудностях а невыгодах нитрования толуола в тринитротолуол в одну фазу .
Образование значительных количеств жета-замещенных продуктов при алкилировании толуола и других монозамещенных бензолов можно объяснить высокой реакционной способностью атакующего реагента. Поскольку бромирование является примером достаточно мягкой реакции замещения, в данном случае сильно проявляются различия между бензолом и толуолом, а также между мета- и пара-положениями в толуоле.
Нитрование менее селективно, чем бромирование изопропилирование значительно менее селективно, чем нитрование. При алкилировании толуола образуется 30% лета-изомера. Более того, при этой реакции становятся незначительными различия между толуолом и бензолом.
Обзор реакций замещения в ароматическом ряду позволяет провести параллель между селективностью реакций с бензолом и толуолом, с одной стороны, и между мета- и пара-положениями в толуоле - с другой. В обоих случаях селективность уменьшается с увеличением реакционной сиособности атакующего агента 2. Данные табл. 4 иллюстрируют эти положения.70
При рассмотрении приведенных в литературе способов определения толуола представлялось возможным использовать фотометрический метод. Последний нашел широкое применение для определения малых количеств толуола, в частности в сточных водах и в воздухе промышленных предприятий. В основе многих вариантов колориметрических определений толуола - нитрование и последующее взаимодействие полученного нитросоединения со щелочью или аммиаком в различных растворителях ацетоне, спирте, метилэтилкетоне, бутаноле, спирто-эфирной смеси и других.
Зависимо от интенсивности охлаждения и перемешивания прилива-ние толуола продолжается 4-8 час. температуру нитрования поддерживают около 50° и по окончании приливания нагревают еще в течение. % часа при 80-90°. Более длительное и сильное нагревание нецелесообразно, так как после окончания приливания толуола нитрование
вряд ли продолжается.
Например при продолжении нагревания при 90° в течение 2 г час. температура затвердевания динитротолуола повысилась в одном случае с 33,7° только до 35,6°. По окончании нитрования содержимое аппарата охлаждают до температуры несколько более высокой, чем температура. плавления динитропродукта, и передавливают содержимое ии-тратора с помощью сжатого воздуха в одии из освинцованных сепараторов (1,2), смешивая реакционную смесь с таким количеством воды, чтобы разбавление достигало приблизительно 16%. При этом вначале происходит очень сильное выделение окислов азота, для отвода которых требуется достаточно мощная вытяжная труба. После отстаивания в течение нескольких часов при температуре несколько более высокой, чем температура плавления нитропродукта, кислота отделяется от продукта, образующего-верхний слой.377
Рубрики
Выберите рубрику 1. ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА НЕФТИ, ПРИРОДНОГО ГАЗА 3. ОСНОВЫ РАЗРАБОТКИ НЕФТЯНЫХ МЕСТОРОЖДЕНИЙ И ЭКСПЛУАТА 3.1. Фонтанная эксплуатация нефтяных скважин 3.4. Эксплуатация скважин погружными электроцентробежны 3.6. Понятие о разработке нефтяных и газовых скважин 7. МЕТОДЫ ВОЗДЕЙСТВИЯ НА ПРИЗАБОЙНУЮ ЗОНУ ПЛАСТА ОСНОВНЫЕ УЗЛЫ ИСПЫТАТЕЛЯ ПЛАСТОВ ВИНТОВЫЕ ЗАБОЙНЫЕ ДВИГАТЕЛИ АВАРИЙНЫЕ И ОСОБЫЕ РЕЖИМЫ РАБОТЫ ЭЛЕКТРООБОРУДОВАНИЯ АГРЕГАТЫ ДЛЯ РЕМОНТА И БУРЕНИЯ СКВАЖИН АНАЛИЗ ПРИЧИН МАЛОДЕБИТНОСТИ СКВАЖИН АНАЛИЗ ТЕХНОЛОГИЙ КАПИТАЛЬНЫХ РЕМОНТОВ СКВАЖИН Арматура устьевая АСФАЛЬТОСМОЛО-ПАРАФИНОВЫЕ ОТЛОЖЕНИЯ Без рубрики БЕЗДЫМНОЕ СЖИГАНИЕ ГАЗА БЕСШТАНГОВЫЕ СКВАЖИННЫЕ НАСОСНЫЕ УСТАНОВКИ блогун БЛОКИ ЦИРКУЛЯЦИОННЫХ СИСТЕМ. борьба с гидратами БОРЬБА С ОТЛОЖЕНИЕМ ПАРАФИНА В ПОДЪЕМНЫХ ТРУБАХ бурение Бурение боковых стволов БУРЕНИЕ НАКЛОННО НАПРАВЛЕННЫХ И ГОРИЗОНТАЛЬНЫХ СКВАЖИН Бурение скважин БУРИЛЬНАЯ КОЛОННА БУРОВЫЕ АВТОМАТИЧЕСКИЕ СТАЦИОНАРНЫЕ КЛЮЧИ БУРОВЫЕ АГРЕГАТЫ И УСТАНОВКИ ДЛЯ ГЕОЛОГО-РАЗВЕДОЧНОГО БУРЕНИЯ БУРОВЫЕ ВЫШКИ БУРОВЫЕ НАСОСЫ БУРОВЫЕ НАСОСЫ БУРОВЫЕ РУКАВА БУРОВЫЕ УСТАНОВКИ В МНОГОЛЕТНЕМЕРЗЛЫХ ПОРОДАХ (ММП) ВЕНТИЛИ. ВИДЫ НЕОДНОРОДНОСТЕЙ СТРОЕНИЯ НЕФТЯНЫХ ЗАЛЕЖЕЙ Виды скважин ВИНТОВЫЕ ПОГРУЖНЫЕ НАСОСЫ С ПРИВОДОМ НА УСТЬЕ ВЛАГОСОДЕРЖАНИЕ И ГИДРАТЫ ПРИРОДНЫХ ГАЗОВ СОСТАВ ГИДРАТ Влияние различных факторов на характеристики ВЗД ВОПРОСЫ ОПТИМИЗАЦИИ РАБОТЫ СИСТЕМЫ ПЛАСТ — УЭЦН ВЫБОР ОБОРУДОВАНИЯ И РЕЖИМА РАБОТЫ УЭЦН ВЫБОР СТАНКА-КАЧАЛКИ Газлифтная установка ЛН Газлифтная эксплуатация нефтяных скважин Газлифтный способ добычи нефти ГАЗЫ НЕФТЯНЫХ И ГАЗОВЫХ МЕСТОРОЖДЕНИЙ И ИХ СВОЙСТВА ГИДРАТООБРАЗОВАНИЕ В ГАЗОКОНДЕНСАТНЫХ СКВАЖИНАХ ГИДРАТООБРАЗОВАНИЕ В СИСТЕМЕ СБОРА НЕФТИ гидрозащита погружного электродвигателя ГИДРОКЛЮЧ ГКШ-1500МТ гидропоршневой насос Глава 8. СРЕДСТВА И МЕТОДЫ ГРАДУИРОВКИ И ПОВЕРКИ РАСХОДОИЗМЕРИТЕЛЬНЫХ СИСТЕМ ГЛУБИННЫЕ НАСОСЫ Горизонтальное бурение ГОРНО-ГЕОЛОГИЧЕСКИЕ УСЛОВИЯ БУРЕНИЯ НЕФТЯНЫХ И ГАЗОВЫХ СКВАЖИН ГРАНУЛОМЕТРИЧЕСКИЙ (МЕХАНИЧЕСКИЙ) СОСТАВ ПОРОД ДАЛЬНИЙ ТРАНСПОРТ НЕФТИ И ГАЗА ДЕФОРМАЦИОННЫЕ МАНОМЕТРЫ Диафрагменные электронасосы ДИЗЕЛЬ-ГИДРАВЛИЧЕСКИЙ АГРЕГАТ САТ-450 ДИЗЕЛЬНЫЕ И ДИЗЕЛЬ-ГИДРАВЛИЧЕСКИЕ АГРЕГАТЫ ДИНАМОМЕТРИРОВАНИЕ УСТАНОВОК ДНУ С ЛМП КОНСТРУКЦИИ ОАО «ОРЕНБУРГНЕФТЬ» добыча нефти добыча нефти в осложненых условиях ДОБЫЧА НЕФТИ С ПРИМЕНЕНИЕМ ШСНУ ЖИДКОСТНЫЕ МАНОМЕТРЫ ЗАБОЙНЫЕ ДВИГАТЕЛИ Закачка растворов кислот в скважину ЗАПОРНАЯ АРМАТУРА. ЗАЩИТа НЕФТЕПРОМЫСЛОВОГО ОБОРУДОВАНИЯ ОТ КОРРОЗИИ ЗАЩИТА ОТ КОРРОЗИИ НЕФТЕПРОМЫСЛОВОГО ОБОРУДОВАНИЯ ИЗМЕНЕНИЕ КУРСА СТВОЛА СКВАЖИНЫ измерение давления, расхода, жидкости, газа и пара ИЗМЕРЕНИЕ КОЛИЧЕСТВА ЖИДКОСТЕЙ И ГАЗОВ ИЗМЕРЕНИЕ РАСХОДА ЖИДКОСТЕЙ, ГАЗОВ И ПАРОВ ИЗМЕРЕНИЕ УРОВНЯ ЖИДКОСТЕЙ ИЗМЕРЕНИЯ ПРОДУКЦИИ МАЛОДЕБИТНЫХ ИНФОРМАЦИОННЫЕ ТЕХНОЛОГИИ В НЕФТЕГАЗОДОБЫЧЕ ИСПЫТАНИЕ СКВАЖИННЫХ ЭЛЕКТРОНАГРЕВАТЕЛЕЙ Исследование глубинно-насосных скважин ИССЛЕДОВАНИЕ ЭФФЕКТИВНОСТИ кабель УЭЦН капитальный ремонт скважин Комплекс оборудования типа КОС и КОС1 КОНСТРУКЦИЯ ВИНТОВОГО ШТАНГОВОГО НАСОСА КОНСТРУКЦИЯ КЛАПАННОГО УЗЛА коррозия Краны. КРЕПЛЕНИЕ СКВАЖИН КТППН МАНИФОЛЬДЫ Маятниковая компоновка Меры безопасности при приготовлении растворов кислоты МЕТОДИКА РАСЧЕТА БУРИЛЬНЫХ КОЛОНН МЕТОДЫ БОРЬБЫ С ОТЛОЖЕНИЯМИ ПАРАФИНА В ФОНТАННЫХ СКВАЖИНАХ Методы воздействия на призабойную зону для увеличения нефтеотдачи пластов МЕТОДЫ И СРЕДСТВА ИЗМЕРЕНИЯ УРОВНЯ ЖИДКОСТЕЙ Методы изучения разрезов скважин. МЕТОДЫ КОСВЕННЫХ ИЗМЕРЕНИЙ ДАВЛЕНИЯ МЕТОДЫ УДАЛЕНИЯ СОЛЕЙ МЕХАНИЗМЫ ПЕРЕДВИЖЕНИЯ И ВЫРАВНИВАНИЯ БУРОВЫХ УСТАНОВОК МЕХАНИЗМЫ ПЕРЕМЕЩЕНИЯ И ВЫРАВНИВАНИЯ МЕХАНИЗМЫ ПРИ СПУСКО-ПОДЪЕМНЫХ ОПЕРАЦИЙ ПРИ БУРЕНИИ НАГРУЗКИ, ДЕЙСТВУЮЩИЕ НА УСТАНОВКУ Наземное оборудование Насосная эксплуатация скважин НАСОСНО-КОМПРЕССОРНЫЕ ТРУБЫ неоднородный пласт Нефть и нефтепродукты Новости портала НОВЫЕ ТЕХНОЛОГИЧЕСКИЕ И ТЕХНИЧЕСКИЕ ОБЕСПЕЧЕНИЕ ЭКОЛОГИЧЕСКОЙ БЕЗОПАСНОСТИ ПРОЦЕССОВ ДОБЫЧИ ОБОРУДОВАНИЕ ГАЗЛИФТНЫХ СКВАЖИН ОБОРУДОВАНИЕ ДЛЯ МЕХАНИЗАЦИИ СПУСКО-ПОДЪЕМНЫХ ОПЕРАЦИЙ Оборудование для нефти и газа ОБОРУДОВАНИЕ ДЛЯ ОДНОВРЕМЕННОЙ РАЗДЕЛЬНОЙ ЭКСПЛУАТАЦ ОБОРУДОВАНИЕ ДЛЯ ПРЕДУСМОТРЕНИЯ ОТКРЫТЫХ ФОНТАНОВ ОБОРУДОВАНИЕ ОБЩЕГО НАЗНАЧЕНИЯ Оборудование ствола скважины, законченной бурением ОБОРУДОВАНИЕ УСТЬЯ КОМПРЕССОРНЫХ СКВАЖИН ОБОРУДОВАНИЕ УСТЬЯ СКВАЖИНЫ Оборудование устья скважины для эксплуатации УЭЦН ОБОРУДОВАНИЕ ФОНТАННЫХ СКВАЖИН ОБОРУДОВАНИЕ ФОНТАННЫХ СКВАЖИН обработка призабойной зоны ОБРАЗОВАНИЕ ГИДРАТОВ И МЕТОДЫ БОРЬБЫ С НИМИ ОБРАЗОВАНИЕ КРИСТАЛЛОГИДРАТОВ В НЕФТЯНЫХ СКВАЖИНАХ ОБЩИЕ ПОНЯТИЯ О ПОДЗЕМНОМ И КАПИТАЛЬНОМ РЕМОНТЕ ОБЩИЕ ПОНЯТИЯ О СТРОИТЕЛЬСТВЕ СКВАЖИН ОГРАНИЧЕНИЕ ПРИТОКА ПЛАСТОВЫХ ВОД Опасные и вредные физические факторы ОПРЕДЕЛЕНИЕ ДАВЛЕНИЯ НА ВЫХОДЕ НАСОСА ОПРОБОВАНИЕ ПЕРСПЕКТИВНЫХ ГОРИЗОНТОВ ОПТИМИЗАЦИЯ РЕЖИМА РАБОТЫ ШСНУ ОПЫТ ЭКСПЛУАТАЦИИ ДНУ С ГИБКИМ ТЯГОВЫМ ЭЛЕМЕНТОМ ОСВОЕНИЕ И ИСПЫТАНИЕ СКВАЖИН ОСВОЕНИЕ И ПУСК В РАБОТУ ФОНТАННЫХ СКВАЖИН ОСЛОЖНЕНИЯ В ПРОЦЕССЕ УГЛУБЛЕНИЯ СКВАЖИНЫ ОСНОВНЫЕ ПОНЯТИЯ И ПОЛОЖЕНИЯ ОСНОВНЫЕ ПОНЯТИЯ И ПОЛОЖЕНИЯ ОСНОВНЫЕ СВЕДЕНИЯ О НЕФТЯНЫХ, ГАЗОВЫХ И ГАЗОКОНДЕНСАТНЫ ОСНОВЫ ГИДРАВЛИЧЕСКИХ РАСЧЕТОВ В БУРЕНИИ ОСНОВЫ НЕФТЕГАЗОДОБЫЧИ ОСНОВЫ ПРОЕКТИРОВАНИЯ НАПРАВЛЕННЫХ СКВАЖИН ОСНОВЫ ПРОМЫШЛЕННОЙ БЕЗОПАСНОСТИ ОЧИСТКА БУРЯЩЕЙСЯ СКВАЖИНЫ ОТ ШЛАМА ОЧИСТКА ПОПУТНЫХ ГАЗОВ пайка и наплавка ПАКЕР ГИДРОМЕХАНИЧЕСКИЙ ДВУХМАНЖЕТНЫЙ ПГМД1 ПАКЕРЫ ГИДРОМЕХАНИЧЕСКИЕ, ГИДРАВЛИЧЕСКИЕ И МЕХАНИЧЕСКИЕ ПАКЕРЫ ДЛЯ ИСПЫТАНИЯ КОЛОНН ПАКЕРЫ РЕЗИНОВО-МЕТАЛЛИЧЕСКОГО ПЕРЕКРЫТИЯ ПРМП-1 ПАКЕРЫ И ЯКОРИ ПАРАМЕТРЫ И КОМПЛЕКТНОСТЬ ЦИРКУЛЯЦИОННЫХ СИСТЕМ Параметры талевых блоков для работы с АСП ПЕРВИЧНОЕ ВСКРЫТИЕ ПРОДУКТИВНЫХ ПЛАСТОВ ПЕРВИЧНЫЕ СПОСОБЫ ЦЕМЕНТИРОВАНИЯ ПЕРЕДВИЖНЫЕ НАСОСНЫЕ УСТАНОВКИ И АГРЕГАТЫ ПЕРЕРАБОТКА ЛОВУШЕЧНЫХ НЕФТЕЙ (НЕФТЕШЛАМОВ) ПЕРИОДИЧЕСКИЙ ГАЗЛИФТ ПЕРСПЕКТИВЫ ИСПОЛЬЗОВАНИЯ ДНУ ПОВЫШЕНИЕ ЭФФЕКТИВНОСТИ ПОВЫШЕНИЕ ЭФФЕКТИВНОСТИ РАБОТЫ ШСНУ Погружение насосов под динамический уровень Подземное оборудование фонтанных скважин ПОДЪЕМ ВЯЗКОЙ ЖИДКОСТИ ПО ЗАТРУБНОМУ ПРОСТРАНСТВУ СКВАЖИНЫ ПОРОДОРАЗРУШАЮЩИЕ ИНСТРУМЕНТЫ ПОРШНЕВЫЕ МАНОМЕТРЫ Потери давления при движении жидкости по нкт Правила безопасности при эксплуатации скважин Правила ведения ремонтных работ в скважинах РД 153-39-023-97 ПРЕДУПРЕЖДЕНИЕ ОБРАЗОВАНИЯ СОЛЕЙ ПРЕДУПРЕЖДЕНИЯ ОБРАЗОВАНИЯ АСПО ПРЕДУПРЕЖДЕНИЯ ОБРАЗОВАНИЯ АСПО при работе ШГН ПРЕИМУЩЕСТВА ДЛИННОХОДОВЫХ Приготовление растворов кислот. ПРИГОТОВЛЕНИЕ, ОЧИСТКА БУРОВЫХ РАСТВОРОВ ПРИМЕНЕНИЕ СТРУЙНЫХ КОМПРЕССОРОВ ДЛЯ УТИЛИЗАЦИИ ПРИМЕНЕНИЕ УЭЦН В СКВАЖИНАХ ОАО «ОРЕНБУРГНЕФТЬ» ПРИНЦИП ДЕЙСТВИЯ И ОСОБЕННОСТИ КОНСТРУКЦИИ ДНУ С ЛМП ПРИЧИНЫ И АНАЛИЗ АВАРИЙ ПРОГНОЗИРОВАНИЕ ОТЛОЖЕНИЯ НОС ПРИ ДОБЫЧЕ НЕФТИ ПРОЕКТИРОВАНИЕ ТРАЕКТОРИИ НАПРАВЛЕННЫХ СКВАЖИН ПРОЕКТИРОВАНИЕ, ОБУСТРОЙСТВО И АНАЛИЗ РАЗРАБОТКИ УГЛЕВОДОРОДНЫХ МЕСТОРОЖДЕНИЙ Производительность насоса ПРОМЫВКА СКВАЖИН И БУРОВЫЕ РАСТВОРЫ ПРОМЫСЛОВЫЕ ИССЛЕДОВАНИЯ ПРОМЫСЛОВЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ ЗОН ОБРАЗОВАНИЯ НОС ПРОМЫСЛОВЫЙ СБОР И ПОДГОТОВКА НЕФТИ, ГАЗА И ВОДЫ ПРОТИВОВЫБРОСОВОЕ ОБОРУДОВАНИЕ ПУТИ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ЭКСПЛУАТАЦИИ СКВАЖИН РАЗМЕЩЕНИЕ ЭКСПЛУАТАЦИОННЫХ И НАГНЕТАТЕЛЬНЫХ СКВАЖИН НА Разное РАЗРУШЕНИЕ ГОРНЫХ ПОРОД РАСПРЕДЕЛЕНИЕ ОБРЫВОВ ПО ДЛИНЕ КОЛОННЫ ШТАНГ РАСЧЕТ ДНУ РАСЧЕТ ПРОИЗВОДИТЕЛЬНОСТИ ДНУ Регулирование свойств цементного раствора и камня с помощью реагентов Режимы добывающих и нагнетательных скважин. РЕЗЕРВЫ СНИЖЕНИЯ ЭНЕРГОПОТРЕБЛЕНИЯ ПРИ ЭКСПЛУАТАЦИ РЕМОНТЫ ПО ЭКОЛОГИЧЕСКОМУ ОЗДОРОВЛЕНИЮ ФОНДА СКВАЖИН РОЛЬ ФОНТАННЫХ ТРУБ САМОХОДНЫЕ УСТАНОВКИ С ПОДВИЖНЫМ… СЕТКА РАЗМЕЩЕНИЯ СКВАЖИН СИСТЕМЫ УЛАВЛИВАНИЯ ЛЕГКИХ УГЛЕВОДОРОДОВ Скважинные уплотнители (пакеры) Скважинные центробежные насосы для добычи нефти СОСТАВ И НЕКОТОРЫЕ СВОЙСТВА ВОД НЕФТЯНЫХ И ГАЗОВЫХ МЕСТ СПЕЦИАЛЬНЫЙ НЕВСТАВНОЙ ШТАНГОВЫЙ НАСОС СПОСОБЫ ДОБЫЧИ НЕФТИ, ПРИМЕНЯЕМЫЕ НА МЕСТОРОЖДЕНИЯХ ОАО СПОСОБЫ ОЦЕНКИ СОСТОЯНИЯ ПЗП СРАВНИТЕЛЬНЫЕ ИСПЫТАНИЯ НАСОСНЫХ УСТАНОВОК СРЕДСТВА И МЕТОДЫ ПОВЕРКИ СЧЕТЧИКОВ КОЛИЧЕСТВА ГАЗОВ СРЕДСТВА И МЕТОДЫ ПОВЕРКИ СЧЕТЧИКОВ КОЛИЧЕСТВА ЖИДКОСТЕЙ СТАДИИ РАЗРАБОТКИ МЕСТОРОЖДЕНИЙ Станки-качалки Струйные насосы струйный насос СЧЕТЧИКИ КОЛИЧЕСТВА ГАЗОВ СЧЕТЧИКИ КОЛИЧЕСТВА ЖИДКОСТЕЙ ТАЛЕВЫЕ МЕХАНИЗМЫ ТЕМПЕРАТУРА И ДАВЛЕНИЕ В ГОРНЫХ ПОРОДАХ И СКВАЖИНАХ Теоретические основы безопасности ТЕХНИКА ИЗМЕРЕНИЯ РАСХОДА Техническая физика ТРАЕКТОРИЮ ПЕРЕМЕЩЕНИЯ ЗАБОЯ СКВАЖИНЫ Трубы УКАЗАНИЯ ПО РАСЧЕТУ ТОКОВ КОРОТКОГО ЗАМЫКАНИЯ УСЛОВИЯ ПРИТОКА ЖИДКОСТИ И ГАЗА В СКВАЖИНЫ Установки гидропоршневых насосов для добычи нефти Установки погружных винтовых электронасосов Установки погружных диафрагменных электронасосов Устьевое оборудование УТЯЖЕЛЕННЫЕ БУРИЛЬНЫЕ ТРУБЫ УЭЦН уэцн полностью ФАКТОРЫ, ВЛИЯЮЩИЕ НА ИНТЕНСИВНОСТЬ ОБРАЗОВАНИЯ АСПО Физико-механические свойства пород-коллекторов ФИЗИЧЕСКАЯ ХАРАКТЕРИСТИКА ГАЗОВ НЕФТЯНЫХ И ГАЗОВЫХ МЕСТ ФИЛЬТРЫ Фонтанный способ добычи нефти ЦЕМЕНТИРОВАНИЕ СКВАЖИН ЦИРКУЛЯЦИОННЫЕ СИСТЕМЫ БУРОВЫХ УСТАНОВОК Шлакопесчаные цементы Шлакопесчаные цементы совместного помола Штанги насосные (ШН) ШТАНГОВЫЕ НАСОСНЫЕ УСТАНОВКИ (ШСНУ) ШТАНГОВЫЕ НАСОСЫ ДЛЯ ПОДЪЕМА ВЯЗКОЙ НЕФТИ ШТАНГОВЫЕ СКВАЖИННЫЕ НАСОСЫ Штанговые скважинные насосы ШСН ЭКСПЛУАТАЦИЯ ГАЗОВЫХ СКВАЖИН эксплуатация малодебитных скважин ЭКСПЛУАТАЦИЯ МАЛОДЕБИТНЫХ СКВАЖИН НА НЕПРЕРЫВНОМ РЕЖИМЕ ЭКСПЛУАТАЦИЯ ОБВОДНЕННЫХ ПАРАФИНСОДЕРЖАЩИХ СКВАЖИН ЭКСПЛУАТАЦИЯ СКВАЖИН ЭКСПЛУАТАЦИЯ СКВАЖИН УЭЦН ЭЛЕКТРОДЕГИДРАТОР. ЭЛЕКТРОДИАФРАГМЕННЫЙ НАСОС энергосбережение скважинного электронасосного агрегата ЯКОРИПоговорим о том, как осуществляется нитрование толуола. Получают подобным взаимодействием огромное количество полуфабрикатов, используемых в изготовлении взрывчатых веществ, фармацевтических препаратов.
Значимость нитрования
Производные бензола в виде ароматических нитросоединений выпускаются в современной химической промышленности. Нитробензол является полупродуктом в анилинокрасочном, парфюмерном, фармацевтическом производстве. Он является отличным растворителем для многих органических соединений, включая и нитрит целлюлозы, формируя с ним желатинообразную массу. В нефтяной промышленности его применяют в качестве очистителя для смазочных масел. При нитровании толуола получают бензидин, анилин, фенилендиамин.
Характеристика нитрования
Нитрование характеризуется вводом группы NO2 в молекулу органического соединения. В зависимости от исходного вещества протекает данный процесс по радикальному, нуклеофильному, электрофильному механизму. В качестве активных частиц выступают катионы нитрония, ионы и радикалы NO2. Реакция нитрования толуола относится к замещению. Для других органических веществ возможно заместительное нитрование, а также присоединение по двойной связи.
Нитрование толуола в молекуле ароматического углеводорода осуществляется с помощью нитрующей смеси (серной и азотной кислот). Каталитические свойства проявляет выступающая в данном процессе в качестве водотнимающего средства.

Уравнение процесса
Нитрование толуола предполагает замещение одного водородного атома нитрогруппой. Как выглядит схема протекающего процесса?
Для того чтобы описать нитрование толуола, уравнение реакции можно представить в следующем виде:
ArH + HONO2+ = Ar-NO2 +H2 O
Оно позволяет судить только об общем ходе взаимодействия, но не раскрывает всех особенностей данного процесса. На самом деле происходит реакция между ароматическими углеводородами и продуктами азотной кислоты.
Учитывая, что в продуктах есть молекулы воды, это приводит к снижению концентрации азотной кислоты, поэтому нитрование толуола замедляется. Для того чтобы избежать подобной проблемы, осуществляют данный процесс при невысоких температурах, используя азотную кислоту в избыточном количестве.
Помимо серной кислоты, в качестве водоотнимающих средств применяют полифосфорные кислоты, трехфтористый бор. Они дают возможность снизать расход азотной кислоты, повышают эффективность взаимодействия.

Нюансы процесса
Нитрование толуола было описано в конце девятнадцатого века В. Марковниковым. Ему удалось установить связь между присутствием в реакционной смеси и скоростью протекания процесса. В современном производстве нитротолуола применяют безводную азотную кислоту, взятую в некотором избытке.
Кроме того, сульфирование и нитрование толуола связано с использованием доступного водоотнимающего компонента фторида бора. Его введение в реакционный процесс позволяет снижать стоимость получаемого продукта, что делает доступным нитрование толуола. Уравнение протекающего процесса в общем виде представлено ниже:
ArH + HNO3 + BF3= Ar-NO2 + BF3 ·H2 O
После завершения взаимодействия вводят воду, благодаря чему моногидрат фторида бора образует дигидрат. Его отгоняют в вакууме, затем добавляют фтористый кальций, возвращая соединение в исходный вид.

Специфика нитрования
Есть некоторые особенности данного процесса, связанные с выбором реагентов, субстракта реакции. Рассмотрим некоторые их варианты подробнее:
- 60-65 процентная азотная кислота в смеси с 96 процентной серной кислотой;
- смесь 98 % азотной кислоты и концентрированной серной кислот подходит для мало реакционных органических веществ;
- нитрат калия или аммония с концентрированной серной кислотой - это отличный выбор для производства полимерных нитросоединений.

Кинетика нитрования
Взаимодействующие со смесью серной и азотной кислот, нитруются по ионному механизму. В. Марковникову удалось охарактеризовать специфику данного взаимодействия. Процесс протекает в несколько стадий. Сначала образуется нитросерная кислота, которая подвергается диссоциации в водном растворе. Ионы нитрония вступают во взаимодействие с толуолом, образуя в качестве продукта нитротолуол. При добавлении в смесь молекул воды происходит замедление процесса.
В растворителях с органической природой - нитрометане, ацетонитриле, сульфолане - образование этого катиона позволяет увеличивать скорость нитрования.
Полученный катион нитрония прикрепляется к ядру ароматического толуола, при этом образуется промежуточное соединение. Далее происходит отрыв протона, приводящий к формированию нитротолуола.
Для детального описания происходящего процесса можно рассмотреть образование «сигма» и «пи» комплексов. Образование «сигма» комплекса является лимитирующей стадией взаимодействия. будет напрямую связана с быстротой присоединения катиона нитрония к атому углерода в ядре ароматического соединения. Отщепление протона от толуола осуществляется практически мгновенно.
Только в некоторых ситуациях могут возникать какие-то проблемы с замещением, связанные с существенным первичным кинетическим изотопным эффектом. Это связано с ускорением обратного процесса при наличии препятствий разного вида.
При выборе в качестве катализатора и водоотнимающего средства концентрированной серной кислоты наблюдается смещение равновесия процесса в сторону образования продуктов реакции.

Заключение
При нитровании толуола образуется нитротолуол, который является является ценным продуктом химической промышленности. Именно это вещество является взрывчатым соединением, поэтому востребовано на взрывных работах. Среди экологических проблем, связанных с его промышленным изготовлением, отметим использование существенного количества концентрированной серной кислоты.
Для того чтобы справиться с такой проблемой, химики ищут способы уменьшения сернокислотных отходов, получаемых после проведения процесса нитрования. Например, процесс осуществляют при пониженных температурах, применяют легко регенерируемые среды. Серная кислота обладает сильными окислительными свойствами, что негативно отражается на коррозии металлов, представляет повышенную опасность для живых организмов. При соблюдении всех норм безопасности можно справиться с этими проблемами, получать нитросоединения высокого качества.
а) Нитрование бензола (тяга!). В маленькой колбе смешивают 4 мл концентрированной серной кислоты ( =1,84) с 3 мл концентрированной азотной кислоты ( =1,4). К полученной смеси приливают по каплям 3 мл бензола, сильно встряхивая содержимое колбы (температура не должна подниматься выше 40 С), охлаждая в случае необходимости водой. Закрыв колбу пробкой с воздушным холодильником, нагревают ее 15 мин на водяной бане до 60 0 С, часто встряхивая. Затем реакционную смесь охлаждают и выливают в стакан с 20 мл ледяной воды, при этом образуются два слоя. Водный слой сливают, а выпавшее на дне масло (нитробензол) еще дважды промывают водой. После отделения от воды сырой нитробензол переливают в сухую пробирку, добавляют 2-3 кусочка прокаленного СаС1 2 и нагревают на водяной бане, пока нитробензол не станет прозрачным. Перегоняют нитробензол из маленькой колбы Вюрца или пробирки с нисходящей трубкой при 207-210 0 С. (Перегонять нитробензол досуха нельзя! Возможен взрыв!).
Напишите уравнение нитрования бензола. Какова роль серной кислоты при нитровании ароматических соединений? Объясните механизм нитрования ароматических соединений.
в) Нитрование толуола. При нитровании толуола возможно образование смеси орто- и пара - нитротолуолов. Контроль за процессом и идентификацию продуктов реакции можно проводить методом тонкослойной хроматографии. Хроматографирование проводят на силуфолевой пластинке, применяя четыреххлористый углерод в качестве элюента. Готовят нитрующую смесь из 3 мл концентрированной азотной кислоты ( =1,1) и 1 мл концентрированной серной кислоты. В пробирку с 2 мл толуола по каплям при охлаждении и встряхивании реакционной смеси добавляют нитрующую смесь. Затем пробирку закрывают пробкой с вертикальной трубкой и нагревают на водяной бане, часто встряхивая. Через 10 мин капилляром отбирают пробу реакционной массы и на стартовую линию силуфолевой пластинки наносят пробу раствора и «свидетелей» орто - и пара- нитротолуолов (в толуоле). Пластинку опускают в камеру с четыреххлористым углеродом и отмечают появление нитротолуолов.
Следующую пробу раствора отбирают через 40 мин, а третью - через 1 ч. Отмечают изменение состава реакционной среды.
Нитрование
Реакция нитрования является одной из наиболее изученных реакций ароматического замещения. Для препаративных целей нитрование, как правило, проводят смесью концентрированных азотной и серной кислот, так называемой нитрующей смесью . На первой стадии реакции происходит образование иона нитрония + NO 2 , который и является электрофильным агентом:
HO-NO 2 + H 2 SO 4 H 2 O + -NO 2 + HSO 4 -
H 2 O + -NO 2 + H 2 SO 4 H 3 O + + HSO 4 - + + NO 2
Наличие иона нитрония в этом растворе подтверждено спектроскопически. Азотная кислота в концентрированной серной кислоте практически нацело превращается в нитроний-катион. Незначительная эффективность самой азотной кислоты в реакции нитрования бензола объясняется низким содержанием иона + NO 2 .
B качестве нитрующих агентов используются также другие системы, в которых генерируется либо катион + NO 2 , либо соединение общей формулы NO2-Y где Y - хорошая уходящая группа. Некоторые из таких систем, нашедшие наибольшее применение, представлены в таблице 1 в порядке увеличения их активности.
Таблица 1. Нитрующие реагенты.
| Нитрующий реагент | Метод генерации | Арены, подвергающиеся нитрованию |
| Азотная кислота HO-NO2 |
Фенолы, эфиры фенолов, бифенил | |
| Ацетилнитрат CH 3 C(O)-O-NO 2 | СН 3 СООН + HNO 3 (СН 3 СО) 2 О + HNO 3 | Бензол, алкилбензолы |
| Диоксид азота N 2 O 4 (O=N-O-NO 2) |
Бензол, алкилбензолы | |
| Нитрующая смесь | H 2 SO 4 конц + HNO 3 | Бензол, алкилбензолы, галогенбензолы, бензойная кислота, нитробензол, нафталин |
| Хлорид нитрония Сl-NO 2 |
Бензол, алкилбензолы, нитробензол, | |
| Тетрафторборат нитрония BF 4 -+ NO 2 | HF . 2BF 3 + HNO 3 | Динитробензол |
На примере реакции нитрования алкилбензолов отчетливо прослеживается влияние пространственных факторов на направление электрофильного замещения. Так, при нитровании толуола (метилбензола) орто -изомер образуется в качестве основного продукта, а при переходе к этил-, изо -пропил- и особенно к трет -бутил-бензолу его выход существенно уменьшается (см. табл. 2).
Таблица 2. Влияние пространственых факторов на соотношение орто-, пара-изомеров в реакции нитрования (NO 2 +)
Замещение в положения, % |
|||
C 6 H 5 -C 2 H 5 |
|||
C 6 H 5 -CH(CH 3) 2 |
|||
C 6 H 5 -C(CH 3) 3 |
|||
При изучении нитрования алкилбензолов было обнаружено так называемое ипсо-замещение , когда электрофильная атака протекает по тому атому углерода бензольного кольца, которое уже содержит заместитель, например:

В отличие от нитрования, при галогенировании атака ароматического субстрата может осуществляться различными электрофилами. Свободные галогены, например, Cl 2 и Br 2 ,(прим.35) могут легко атаковать активированное ароматическое ядро (например, фенола), но не способны реагировать с бензолами и алкилбензолами (фотохимическая активация может, однако, в последнем случае привести к протеканию радикального замещения в боковую цепь; см. раздел IV.3). Для поляризации атакующей молекулы галогена необходим катализ кислотами Льюиса , такими как AlCl 3 , FeBr 3 , и т.п.; при этом в молекуле галогена появляется так называемый "электрофильный конец" (энергия же, требующаяся для образования катиона Наl + существенно выше). Тем самым электрофильное замещение существенно облегчается:

Галогенирование протекает очень энергично, если использовать реагенты, в которых галоген в результате поляризации имеет сильный положительный заряд или даже существует как катион. Так, очень инертный мета -динитробензол можно пробромировать бромом в концентрированной серной кислоте в присутствии сульфата серебра. Предполагают, что в этом случае промежуточно образуется бром-катион:
2Br 2 + Ag 2 SO 4 2Br + + 2AgBr + SO 4 2-
Реакционная способность элементарного иода в реакциях электрофильного замещения в ароматическом ядре незначительна, так что прямое иодирование возможно только в случае фенола и ароматических аминов. Иодирование других ароматических соединений проводят в присутствии окислителя (обычно, азотной кислоты). Считается, что в этих условиях роль электрофильного агента играет ион I- + OH 2 .

Для галогенирования аренов можно применять также смешанные галогены , например, монохлорид брома (BrCl) или иода (ICl):


Галогенирование in vivo . В качестве примера электрофильного ароматического галогенирования, протекающего в живых организмах, можно привести реакцию иодирования -аминокислоты - тирозина в ходе биосинтеза иодсодержащих гормонов щитовидной железы до 3-иодтирозина и далее до 3,5-дииодтирозина:

Детали механизма сульфирования исследованы менее подробно по сравнению с нитрованием и галогенированием. Сам бензол сульфируется довольно медленно горячей концентрированной серной кислотой, но быстро - олеумом, SO 3 в инертных растворителях или комплексом SO 3 с пиридином. Природа электрофильной частицы зависит от условий реакции, но, вероятно, это всегда SO 3 , или в свободном состоянии, или связанный с "носителем", например, в виде H 2 SO 4 . SO 3 (H 2 S 2 O 7) в серной кислоте. Небольшие количества SO 3 образуются в H 2 SO 4:
2H 2 SO 4 SO 3 + H 3 O + + HSO 4 -
Атаку ароматического субстрата осуществляет атом серы поскольку он сильно положительно поляризован, то есть электронодефицитен:

Сульфирование является обратимым процессом. Это имеет практическое значение: при обработке сульфокислот водяным паромпроисходит замещение группы SO 3 Н на водород. Таким образом, можно ввести группу SO 3 Н как заместитель, ориентирующий требуемым образом последующие реакции (см. раздел IV.1.Б), а затем ее отщепить. Некоторые интересные особенности имеет сульфирование нафталина (см. раздел IV.1.Г).
Подобно галогенам, алкилгалогениды могут быть так сильно поляризованы кислотами Льюиса (хлоридами алюминия и цинка, трифторидом бора и др.), что они становятся способными к электрофильному замещению в ароматическом ядре:
R-Cl + AlCl 3 R +... Cl ...- AlCl 3 R + AlCl 4 -
Кроме алкилгалогенидов, источниками карбокатионов для галогенирования ароматических соединений могут быть алкены или спирты. При этом необходимо присутствие протонной кислоты, чтобы протонировать алкен или спирт. В случае спиртов требуется добавка не менее чем эквимольного количества кислоты (так как вода, выделяющаяся в ходе реакции, дезактивирует эквимольное количество катализатора), тогда как в реакциях с участием алкилгалогенидов и алкенов достаточно добавлять незначительное количество катализатора.
В лаборатории алкилирование по Фриделю-Крафтсу имеет ограниченное применение, так как обычно при этой реакции образуются смеси продуктов, что обусловлено рядом причин:
1) Образующийся продукт алкилирования легче вступает в реакции электрофильного ароматического замещения, чем исходное соединение (Alk - электронодонорная группа), поэтому дальше преимущественно алкилируется продукт. Если хотят получить продукты моноалкилирования, то необходимо брать большой избыток ароматического соединения.
2) Как и сульфирование, реакция алкилирования по Фриделю-Крафтсу обратима (см. также раздел IV.1.Г).
3) Даже в мягких условиях первичные и вторичные алкилгалогениды дают преимущественно вторичные или третичные алкиларены соответственно, поскольку алкилирование происходит в условиях, приближающихся к S N 1 реакции.(прим.37) Перегруппировки можно избежать, если работать при низких температурах.
Ацилирование ароматических соединений по Фриделю-Крафтсу является важнейшим методом синтеза жирноароматических кетонов. Производные карбоновых кислот, такие как ацилгалогениды и ангидриды, имеют полярную карбонильную группу и в принципе способны к электрофильному замещению в ароматических системах:

Электрофильная активность этих соединений, однако, невелика, и должна быть повышена действием кислот Льюиса. При этом кислотный катализатор, как правило, атакует атом кислорода карбонильного соединения и, смещая электронную плотность, повышает положительный заряд соседнего атома углерода. В результате образуется поляризованный комплекс (а в пределе - ацилкатион), действующий как электрофил:

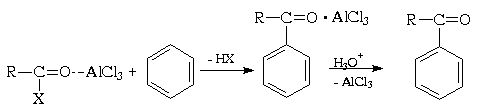
Важное отличие реакции ацилирования ацилгалогенидами от реакции алкилирования алкилгалогенидами состоит в том, что в первой из этих реакций требуется более 1 моль кислоты Льюиса , тогда как во второй необходимо только каталитические количество. Это обусловлено тем, что кислота Льюиса образует комплекс как с ацилирующим производным карбоновой кислоты, так и с кетоном - продуктом реакции. При взаимодействии с ангидридами получающаяся кислота связывает еще моль моль катализатора, так что в целом его необходимо по крайней мере два моль. В каждом случае по окончании реакции образовавшийся комплекс кетона с хлоридом алюминия (или другой кислотой Льюиса) должен быть гидролитически разрушен (соляной кислотой со льдом).
Полиацилирования не наблюдается, поскольку образующийся кетон значительно менее реакционноспособен, чем исходное соединение (см. раздел IV.1.Б). Поэтому алкилбензолы часто предпочитают получать не прямым алкилированием, а ацилированием по Фриделю-Крафтсу с последующим восстановлением. Ароматические соединения с сильнодезактивирующими заместителями, например, нитро- или циано- группами, также не ацилируются по Фриделю-Крафтсу.
Контрольные задачи
2. Изобразите диаграмму потенциальной энергии
для реакции электрофильного ароматического
замещения, в которой медленной стадией является
образование
-комплекса (например,
нитрование бензола борфторидом нитрония;
см. раздел IV.1.A).
3. Какой продукт преимущственно образуется при бромировании: а)пара -нитротолуола; б) мета -нитробензолсульфокислоты; в) орто -нитрофенола.
4. Адреналин (1-(3",4"-дигидроксифенил)-2-метиламиноэтанол)- первый гормон, выделенный из мозгового вещества надпочечников, в настоящее время синтезируюют в три стадии из пирокатехина. Напишите уравнение первой стадии этого синтеза - реакции ацилирования пирокатехина (1,2-дигидроксибензола) хлорангидридом хлоруксусной киcлоты и объясните механизм).
5. Одной их качественных реакций на белки является ксантопротеиновая реакция, указывающая на присутствие ароматических -аминокислот. Она заключается в обработке белка азотной кислотой при нагревании. Напишите уравнение ксантопротеиновой реакции с тирозином (см. раздел I), образовавшимся в результате гидролиза белка.
Физические свойства
Бензол и его ближайшие гомологи – бесцветные жидкости со специфическим запахом. Ароматические углеводороды легче воды и в ней не растворяются, однако легко растворяются в органических растворителях – спирте, эфире, ацетоне.
Бензол и его гомологи сами являются хорошими растворителями для многих органических веществ. Все арены горят коптящим пламенем ввиду высокого содержания углерода вих молекулах.
Физические свойства некоторых аренов представлены в таблице.
Таблица. Физические свойства некоторых аренов
|
Название |
Формула |
t°.пл., |
t°.кип., |
|
Бензол |
C 6 H 6 |
5,5 |
80,1 |
|
Толуол (метилбензол) |
С 6 Н 5 СH 3 |
95,0 |
110,6 |
|
Этилбензол |
С 6 Н 5 С 2 H 5 |
95,0 |
136,2 |
|
Ксилол (диметилбензол) |
С 6 Н 4 (СH 3) 2 |
||
|
орто- |
25,18 |
144,41 |
|
|
мета- |
47,87 |
139,10 |
|
|
пара- |
13,26 |
138,35 |
|
|
Пропилбензол |
С 6 Н 5 (CH 2) 2 CH 3 |
99,0 |
159,20 |
|
Кумол (изопропилбензол) |
C 6 H 5 CH(CH 3) 2 |
96,0 |
152,39 |
|
Стирол (винилбензол) |
С 6 Н 5 CH=СН 2 |
30,6 |
145,2 |
Бензол – легкокипящая ( t кип = 80,1°С), бесцветная жидкость, не растворяется в воде
Внимание! Бензол – яд, действует на почки, изменяет формулу крови (при длительном воздействии), может нарушать структуру хромосом.
Большинство ароматических углеводородов опасны для жизни, токсичны.
Получение аренов (бензола и его гомологов)
В лаборатории
1. Сплавление солей бензойной кислоты с твёрдыми щелочами
C 6 H 5 -COONa + NaOH t → C 6 H 6 + Na 2 CO 3
бензоат натрия
2. Реакция Вюрца-Фиттинга : (здесь Г – галоген)
С 6 H 5 -Г + 2 Na + R -Г → C 6 H 5 - R + 2 Na Г
С 6 H 5 -Cl + 2Na + CH 3 -Cl → C 6 H 5 -CH 3 + 2NaCl
В промышленности
- выделяют из нефти и угля методом фракционной перегонки, риформингом;
- из каменноугольной смолы и коксового газа
1. Дегидроциклизацией алканов с числом атомов углерода больше 6:
C 6 H 14 t , kat →C 6 H 6 + 4H 2
2. Тримеризация ацетилена (только для бензола) – р. Зелинского :
3С 2 H 2 600° C , акт. уголь →C 6 H 6
3. Дегидрированием циклогексана и его гомологов:
Советский академик Николай Дмитриевич Зелинский установил, что бензол образуется из циклогексана (дегидрирование циклоалканов
C 6 H 12 t, kat →C 6 H 6 + 3H 2

C 6 H 11 -CH 3 t , kat →C 6 H 5 -CH 3 + 3H 2
метилциклогексантолуол
4. Алкилирование бензола (получение гомологов бензола) – р Фриделя-Крафтса .
C 6 H 6 + C 2 H 5 -Cl t, AlCl3 →C 6 H 5 -C 2 H 5 + HCl
хлорэтан этилбензол

Химические свойства аренов
I . РЕАКЦИИ ОКИСЛЕНИЯ
1. Горение (коптящее пламя):
2C 6 H 6 + 15O 2 t →12CO 2 + 6H 2 O + Q
2. Бензол при обычных условиях не обесцвечивает бромную воду и водный раствор марганцовки
3. Гомологи бензола окисляются перманганатом калия (обесцвечивают марганцовку):
А) в кислой среде до бензойной кислоты
При действии на гомологи бензола перманганата калия и других сильных окислителей боковые цепи окисляются. Какой бы сложной ни была цепь заместителя, она разрушается, за исключением a -атома углерода, который окисляется в карбоксильную группу.
Гомологи бензола с одной боковой цепью дают бензойную кислоту:
Гомологи, содержащие две боковые цепи, дают двухосновные кислоты:
5C 6 H 5 -C 2 H 5 + 12KMnO 4 + 18H 2 SO 4 → 5C 6 H 5 COOH + 5CO 2 + 6K 2 SO 4 + 12MnSO 4 +28H 2 O
5C 6 H 5 -CH 3 + 6KMnO 4 + 9H 2 SO 4 → 5C 6 H 5 COOH + 3K 2 SO 4 + 6MnSO 4 +14H 2 O
Упрощённо:
C 6 H 5 -CH 3 + 3O KMnO4 →C 6 H 5 COOH + H 2 O
Б) в нейтральной и слабощелочной до солей бензойной кислоты
C 6 H 5 -CH 3 + 2KMnO 4 → C 6 H 5 COO К + K ОН + 2MnO 2 + H 2 O
II . РЕАКЦИИ ПРИСОЕДИНЕНИЯ (труднее, чем у алкенов)
1. Галогенирование
C 6 H 6 +3Cl 2 h ν → C 6 H 6 Cl 6 (гексахлорциклогексан - гексахлоран)
2. Гидрирование
C 6 H 6 + 3H 2 t , Pt или Ni →C 6 H 12 (циклогексан)
3. Полимеризация
III . РЕАКЦИИ ЗАМЕЩЕНИЯ – ионный механизм(легче, чем у алканов)
1. Галогенирование -
a ) бензола
C 6 H 6 + Cl 2 AlCl 3 → C 6 H 5 -Cl + HCl (хлорбензол)
C 6 H 6 + 6Cl 2 t ,AlCl3 →C 6 Cl 6 + 6HCl ( гексахлорбензол )
C 6 H 6 + Br 2 t,FeCl3 → C 6 H 5 -Br + HBr ( бромбензол )
б) гомологов бензола при облучении или нагревании
По химическим свойствам алкильные радикалы подобны алканам. Атомы водорода в них замещаются на галоген по свободно-радикальному механизму. Поэтому в отсутствие катализатора при нагревании или УФ-облучении идет радикальная реакция замещения в боковой цепи. Влияние бензольного кольца на алкильные заместители приводит к тому, что замещается всегда атом водорода у атома углерода, непосредственно связанного с бензольным кольцом (a -атома углерода).
1) C 6 H 5 -CH 3 + Cl 2 h ν → C 6 H 5 -CH 2 -Cl + HCl
в) гомологов бензола в присутствии катализатора
C 6 H 5 -CH 3 + Cl 2 AlCl 3 → (смесь орта, пара производных) +HCl
2. Нитрование (с азотной кислотой)
C 6 H 6 + HO-NO 2 t, H2SO4 →C 6 H 5 -NO 2 + H 2 O
нитробензол - запах миндаля !
C 6 H 5 -CH 3 + 3HO-NO 2 t, H2SO4 → С H 3 -C 6 H 2 (NO 2) 3 + 3H 2 O2,4,6-тринитротолуол (тол, тротил)
Применение бензола и его гомологов
Бензол C 6 H 6 – хороший растворитель. Бензол в качестве добавки улучшает качество моторного топлива. Служит сырьем для получения многих ароматических органических соединений – нитробензола C 6 H 5 NO 2 (растворитель, из него получают анилин), хлорбензола C 6 H 5 Cl, фенола C 6 H 5 OH, стирола и т.д.
Толуол C 6 H 5 –CH 3 – растворитель, используется при производстве красителей, лекарственных и взрывчатых веществ (тротил (тол), или 2,4,6-тринитротолуол ТНТ).
Ксилолы C 6 H 4 (CH 3) 2 . Технический ксилол – смесь трех изомеров (орто -, мета - и пара -ксилолов) – применяется в качестве растворителя и исходного продукта для синтеза многих органических соединений.
Изопропилбензол C 6 H 5 –CH(CH 3) 2 служит для получения фенола и ацетона.
Хлорпроизводные бензола используют для защиты растений. Так, продукт замещения в бензоле атомов Н атомами хлора – гексахлорбензол С 6 Сl 6 – фунгицид; его применяют для сухого протравливания семян пшеницы и ржи против твердой головни. Продукт присоединения хлора к бензолу – гексахлорциклогексан (гексахлоран) С 6 Н 6 Сl 6 – инсектицид; его используют для борьбы с вредными насекомыми. Упомянутые вещества относятся к пестицидам – химическим средствам борьбы с микроорганизмами, растениями и животными.
Стирол C 6 H 5 – CH = CH 2 очень легко полимеризуется, образуя полистирол, а сополимеризуясь с бутадиеном – бутадиенстирольные каучуки.
ВИДЕО-ОПЫТЫ

 Вход
Вход